Лекарственные растения

Каштан конский
Aesculus hippocastanum
Таксон: семейство Конскокаштановые (Hippocastanaceae)
Другие названия: конский каштан обыкновенный
English: Horse-chesnut
Ботаническое описание каштана конского
Каштан конский - высокое (до 30 м) листопадное дерево с широкой густой кроной. Листья супротивные, длинночерешковые, пальчатосложные с 5–7 сидячими обратнояйцевидными вытянуто-заостренными листьями. Цветки неправильные, белые с красно-розовыми пятнышками, собранные в прямостоячие пирамидальные метелки. Цветет в мае. Плод — круглая коробочка диаметром до 6 см, покрытая большими мягкими шипами, внутри которой 1–2 больших коричневых блестящих семени. Плоды созревают в сентябре–октябре.
Распространение
Каштан конский в дикой природе встречается как реликтовое растение в горных лесах Балканского полуострова (на севере Греции, Албании, Республики Македонии, Сербии и Болгарии). В Европе и России культивируется с XVI в. в садах и парках как декоративное растение.
Каштан конский теневынослив, хорошо растёт на глубоких рыхлых почвах — глинистых или супесчаных, достаточно влажных, но без избыточного увлажнения. Переносит довольно сухие чернозёмные почвы в степной зоне, засолённые почвы переносит плохо. Чувствителен к суховеям, отчего листья часто летом сильно обгорают и преждевременно опадают.
Зимостоек в культуре в средней полосе Европейской части России (до Москвы). На широте Москвы в очень суровые зимы подмерзает; молодые деревья подмерзают и в Санкт-Петербурге, но в защищённых местах вырастают в крупные, обильно цветущие деревья.
Каштан конский при благоприятных условиях достигает возраста 200—300 лет.
Сбор и заготовка лекарственного сырья каштана конского
С лечебной целью и для изготовления лекарственных препаратов используют кору молодых ветвей (Cortex Aesculi hippocastani), лист (Folium Aesculi hippocastani), цветки (Flores Aesculi hippocastani) и плоды (Fructus Aesculi hippocastani) каштана конского. Кору собирают весной, разрезают на куски и сушат сразу после сбора на открытом воздухе или в хорошо проветриваемом помещении. Цветки заготавливают в мае, сушат первый день на солнце, а затем — под навесом или в помещении. Листья каштана конского заготавливают с мая по сентябрь, до пожелтения, с черешками или без них. Сушат на свежем воздухе под навесом или в хорошо проветриваемом помещении, расстилая тонким слоем (2–3 см). Собирают полностью созревшие плоды, когда они начинают опадать. Сушат их под навесом или в хорошо проветриваемом помещении при температуре до 25°С.
Биологически активные вещества мелиссы
Фармакологическая активность плодов каштана конского связана с содержанием кумаринового гликозида эскулина (эскулозида) и его агликона эскулетина (эсцинола), оксикумаринового гликозида фраксина и его агликона фраксетина, а также тритерпенового сапонинового гликозида β-амиринового типа эсцина (содержание до 13%).
Дальнейший химический анализ показал, что эсцин является смесью нескольких веществ: α-эсцина, β-эсцина и криптоэсцина (H. Wagner и соавт., 1970), или эсцинов Ia, Ib, IIa, IIb и IIIa (N. Murakami и соавт., 1994), агликонами которых является эсцигенин, протоэсцигенин, барингтогенины С и D.
В плодах каштана конского найдены также эсцины IIIb, IV, V и VI, изоэсцины Ia, Ib и V (M. Yoshikawa и соавт., 1998). Основным компонентом, определяющим биологическую активность эсцина, является β-эсцин. При исследовании препарата эсцин (производства АО «Галычфарм») методом жидкостной хроматографии установлено, что содержание β-эсцина в нем составляет 76,35–79,29% (А. В. Шовковый и А. Т. Шеин, 1999). Наряду с эсцином в плодах каштана присутствуют другие сапониновые гликозиды. В частности, при кислотном гидролизе сапониновой фракции получены сапогенолы гипокаэскулин (21-О-ангелоил-22-О-тиглоил-R1-барингенол или 21-О-тиглоил-22-О-ангелоил-R1-барингенол) и барингтогенол-С-21-ангелат (T. Konoshima и K. H. Lee, 1986).
Кроме того, в плодах каштана конского обыкновенного содержится около 0,13% флавоноидных гликозидов (кверцитрина, изокверцитрина, кверцетина и кемпферола), около 0,9% дубильных веществ (катехиновых танинов), жирное масло (5–7%), белки (11%), пектины, крахмал (до 49,5%).
Флавоноидами — производные кемпферола и кверцетина — богаты также цветки и лист каштана. В частности, в листах содержатся 3-глюкозид кемпферола, 3-арабинозид кемпферола, 3-рамноглюкозид кемпферола, кверцитрин, изокверцитрин, рутин и сиреозид. Кроме флавоновых гликозидов, в цветках каштана присутствуют слизь, дубильные и пектиновые вещества, а в листьях — пектиновые вещества и каротиноиды (лютеин, виолаксантин).
В коре каштана конского содержатся кумариновый гликозид эскулин (3%) и его агликон эскулетин, эсцин, оксикумариновые гликозиды фраксин и скополин и их агликоны (фраксетин и скополетин), флавоноид кверцетин, дубильные вещества (в частности, катехиновый димер проантоцианидин-А2), фитостеролы (стигмастерол, α-спинастерол, β-ситостерол), жирное масло (2,5-7%), сахара (9%), аскорбиновая кислота, тиамин, филохинон.
История применения каштана конского в медицине
Первое упоминание о применении каштана с лечебной целью появилось в 1556 г. Врач Петер Андреас Маттиоли (1500–1577) рекомендовал давать плоды каштана конского лошадям, которые страдали одышкой. В 1575 г. ботаник Клаузиус привез из Турции саженцы каштана и высадил их в Вене как декоративные деревья. В 1615 г. каштаны были высажены во Франции, через 200 лет они появились в Америке. С 1842 г. каштанами начали озеленять Киев. Некоторые ботаники того времени считали, что каштан походит из Индии, на что указывает его французское название — «Marronier d’Indе». Только в ХIХ в. было установлено, что родиной каштана являются горные леса Балканского полуострова.
Из поджаренных на горячих камнях ядовитых плодов каштана конского американские индейцы готовили пюре, затем его на протяжении нескольких дней вымачивали в известковой воде и использовали для изготовления муки. Из проращенного семени, которое становится приятным на вкус вследствие преобразования горьких веществ в сладкие, они готовили солод. C. L. Millspaugh (1974) считает, что кожуру семени индейцы использовали как наркотическое вещество (по активности 10 г приравнивалось к 3 г опия). Порошок из семян и измельченных ветвей использовали для отравления рыбы.
В народной медицине стран юга Европы в XVIII-ХIХ вв. плоды и кору каштана применяли как заменитель коры хинного дерева для лечения малярии, лихорадочных состояний и амебной дизентерии. Особенно популярными были эти средства во Франции, что было связано с политической изоляцией страны во время правления Наполеона II и прекращением импорта дорогой хинной коры. Однако, как указывают исторические источники, средства из каштана по действию были более слабыми, чем кора хинного дерева. Позднее появились сообщения, что каштан лечит некоторые заболевания, связанные с нарушением циркуляции крови. Порошком из плодов присыпали варикозные язвы. В 1708 г. Tabler сообщил об эффективности отвара при лечении геморроя. С 1866 г. в аптеках Европы начала появляться настойка каштана, которую назначали при хронических воспалениях кишечника, подагре и геморрое.
В научно-практическую медицину конский каштан ввел французский врач A. Artault de Vevey. В 1896 г. во французском журнале «Revue de thеérap. mеéd. chirur.» появились его публикации об успешном лечении геморроя и варикозного расширения вен настойкой каштана. Известный французский фитотерапевт Леклерк считал каштан эффективным средством для лечения простатитов и аденомы простаты. В 50-х годах ХХ в. началось производство венотонизирующих препаратов каштана в Германии.
Галеновые препараты конского каштана и сегодня широко используются в народной медицине многих стран. Настойка цветков каштана обладает противовоспалительными и обезболивающими свойствами, семя — противовоспалительными, а кожура семени — кровоостанавливающими, противовоспалительными и обезболивающими свойствами. Свежий сок цветков назначают внутрь при варикозном расширении вен, тромбофлебите, атеросклерозе и геморрое. Сок цветков, законсервированный спиртом, настойку цветков или плодов рекомендуют внутрь и местно при варикозном расширении вен и геморрое, в виде втираний — при артритах, ревматических и подагрических болях. Отвар кожуры плодов назначают местно (ванночки, спринцевание) при маточных и геморроидальных кровотечениях. Порошок семени каштана применяют при простудных заболеваниях дыхательных путей.
Отвары и настои коры каштана обладают вяжущими, кровоостанавливающими, противовоспалительными, обезболивающими и противосудорожными свойствами. Их применяют как эффективные внутренние и наружные средства при продолжительной диареи, хронических колитах, повышенной кислотности желудочного сока, заболеваниях дыхательных путей (хронических бронхитах), малярии. Как гемостатическое средство их рекомендуют при геморроидальных и внутренних кровотечениях, особенно маточных.
Настой коры, настойку плодов, настой кожуры плодов и свежую потертую листву каштана используют также как наружное средство — для перевязок нагноившихся ран.
Фармакологические свойства каштана конского
Изучение фармакологической активности галеновых препаратов каштана (спиртового экстракта, спиртовых настоек, отваров и настоев из листа, цветков и плодов) показало, что наиболее эффективным является спиртовой экстракт плодов, обладающий невысокой острой токсичностью.
Экстракт плодов каштана стимулирует сердечную деятельность у холоднокровных животных, снижает на 15–70% артериальное давление у котов, в небольших дозах расширяет сосуды изолированного уха кролика, а в более высоких сужает их. При экспериментальном тромбофлебите у собак экстракт каштана уменьшает общую воспалительную реакцию и местный отек. У людей без патологии периферических кровеносных сосудов было установлено, что экстракт плодов повышает тонус вен голени.
Кроме того, он проявляет противовоспалительные, противоотечные, обезболивающие и капилляроукрепляющие свойства, уменьшает вязкость крови, препятствует развитию стаза в капиллярах.
Очищенный суммарный экстракт плодов каштана конского способствует обратному развитию экспериментального холестеринового атеросклероза у кроликов, нормализует содержание холестерина и лецитина в крови, уменьшает липоидоз аорты и печени.
Фармакологическая активность галеновых препаратов каштана конского связана главным образом с содержанием тритерпенового сапонинового гликозида эсцина и его производных. Как и другие сапонины, эсцин обладает гемолитической активностью, но в терапевтических дозах она не проявляется. В отличие от почти нерастворимой в воде кристаллической β-эсциновой кислоты, водорастворимые эсциновые формы α-эсциновой кислоты, α-эсцинат натрия и аморфная β-эсциновая кислота хорошо всасываются в желудочно-кишечном тракте. β-эсцинат натрия и аморфная β-эсциновая кислота при пероральном введении и эсцин при подкожном введении обладают выраженными противовоспалительными и противоотечными свойствами, улучшают трофику тканей при недостаточном кровоснабжении и отеках.
Противовоспалительные свойства эсцина и его производных подтверждены в многочисленных экспериментах на разных моделях воспаления. Они угнетают развитие экспериментального отека лапы крыс, вызванного овальбумином, гистамином, серотонином, ожогом или застоем (лимфатический отек), аппликацией местнораздражающих веществ (хлороформа) (M. Guillaume и F. Padioleau, 1994). Эсцин дозозависимо уменьшает (максимально на 70%) проницаемость плазмолимфатического барьера, обусловленную инъекцией брадикинина в лапу кролей (M. Rothkopf и G. Vogel, 1976), препятствует возникновению экссудативной реакции на введение простагландинов Е1 и F2a (M. Rothkopf-Ischebeck и G. Vogel, 1980; D. Longiave и соавт., 1978). Аналогичное действие эсцина проявляется на моделях ультрафиолетовой эритемы (R. Eisenburger и соавт., 1976), воспаления слизистой мочевого пузыря крыс, вызванного электрокоагуляцией (P. Strohmenger и H. Wenzel, 1976), постишемического отека мышц и отека мозга, обусловленного холодовой травмой (M. Arnold и M. Przerwa, 1976). Эсцин дозозависимо угнетает развитие формалинового перитонита и каррагинанового плеврита у крыс (Rothkopf и G. Vogel, 1976; M. Guillaume и F. Padioleau, 1994); уменьшает количество экссудата, содержание в нем белка, миграцию лейкоцитов в плевральную полость. Установлено, что при увеличении дозы эсцина более эффективно угнетается экссудация в брюшную полость молекул небольших размеров по сравнению с большими молекулами.
Способность очищенных препаратов эсцинов Ia, Ib, IIa и IIb в дозе 50–200 мг/кг угнетать начальную экссудативную стадию воспаления подтвердили H. Matsuda и соавт. (1997) на разных экспериментальных моделях: воспаление кожи крыс и мышей в ответ на введение уксусной кислоты, овальбумина, декстрана, трипсина, гиалуронидазы, каолина, пчелиного яда, каррагинина, гистамина, брадикинина и при реакции Артюса. Эсцины, за исключением эсцина Іа, препятствуют повышению сосудистой проницаемости под влиянием серотонина. На моделях поздней (пролиферативной) фазы воспаления эффекта не наблюдалось. Тем не менее другие исследователи указывают на способность эсцина и продуктов его гидролиза угнетать развитие ватной гранулемы у крыс (R. Eisenburger и соавт., 1976), реакции на имплантацию пластиковой пены (M. Guillaume и F. Padioleau, 1994; M. Przerwa и M. Arnold, 1975).
Важное значение в развитии антиэкссудативного действия эсцина имеет его способность повышать резистентность сосудов, что доказано на разных моделях воспаления в тесте с синькой Эванса (Rothkopf и G. Vogel, 1976), а также по результатам петехиальной пробы у морских свинок, которые находились на скорбутогенной диете (M. Guillaume и F. Padioleau, 1994). Эсцины, особенно его сапогенин эсцинол, угнетают активность гиалуронидазы (IC50 149,9 мкM и 1,65 мкМ соответственно) (R. M. Facino и соавт., 1995). Таким образом, в основе противовоспалительного действия эсцина лежит укрепление стенок капилляров. Эсцин уменьшает количество пор в стенках капилляров и их диаметр. В опытах на животных установлено, что по антиэкссудативному действию эсцин в 600 раз превосходит классический флавон рутин. Как показано на моделях формалинового перитонита, экспериментального плеврита у крыс и отека лапы кролика, по антиэкссудативному потенциалу эффект эсцина сопоставим с эффектом ацетилсалициловой кислоты, гидрокортизона, фенилбутазона и бутадиона, а в отдельных случаях даже превосходит их. Существует предположение, что противовоспалительное действие эсцина связано с его влиянием на кору надпочечников и способностью стимулировать секрецию глюкокортикоидов.
Эсцин обладает выраженными мембранотропными свойствами. Связываясь с липидами биологических мембран, он увеличивает текучесть липидного бислоя (Л. В. Иванов и соавт., 1988). Учитывая то, что эсцин значительно сильнее связывается с мембранами эритроцитов и клеток сосудистой стенки, чем с липосомами (которые состоят из фосфолипидов), можно предположить также его способность реагировать с мембранными белками. Такое взаимодействие возможно между остатком глюкуроновой кислоты и остатками аминокислот лизина, аргинина. Опыты по изучению текучести липидов сосудистой стенки указывают на то, что увеличение резистентности сосудов в присутствии эсцина происходит вследствие повышения их эластичности и не связано с уплотнением ткани сосудов. Увеличением текучести липидов частично объясняют сосудотонизирующее действие препарата. Мембраностабилизирующий эффект эсцинола, эсцина и эскулозида продемонстрирован в опытах по изучению резистентности эритроцитов к осмотическому гемолизу. Оптимальная действующая концентрация эсцина 10-5 Г отвечала уровню препарата в крови пациентов после приема терапевтической дозы (Л. А. Чайка и И. И. Хаджай, 1977). Эсцин как сапонин уменьшает поверхностное натяжение жидкости, хорошо адсорбируется на границе поверхностей, и эти эффекты распространяются на сосудистую стенку. Эсцин повышает смачиваемость капилляров, что облегчает направленный внутрь капилляра ток тканевой жидкости. Таким образом, жидкость, которая предопределяет периваскулярный отек, в связи с повышенным онкотическим давлением внутри капилляров направляется в сосуды.
Важными механизмами противовоспалительного и противоотечного действия эсцина является также его венотонизирующий эффект. Выраженные венотонизирующие свойства эсцина подтверждены в экспериментальных исследованиях in vitro на портальной и подкожной вене кролей, подкожной вене собак, а также на сегментах нормальной и варикозно расширенной v. saphena человека (ЕС50 9,4–15,9 мкМ/л). При исследовании нормальных и слегка расширенных вен с недостаточностью клапанов полученный эффект составлял 70–71% от максимально возможного сокращения под влиянием KCl и 43% от сокращения, обусловленного норадреналином. Тем не менее вены, глубоко пораженные варикозной болезнью, реагировали на эсцин слабее — венотонизирующий эффект составлял только 10% от максимально возможного (F. Brunner и соавт., 2001). Приведенные результаты подтверждают большую терапевтическую эффективность эсцина на ранних стадиях варикозной болезни. Венотонизирующий эффект эсцина при исследовании сегментов нормальной подкожной вены человека сохранялся в течение часа после удаления препарата из среды инкубации.
По максимальному эффекту эсцин превосходил ацетилхолин и вазопрессин и приравнивался к активности серотонина и дигидроэрготамина. Тем не менее афинность венозной стенки к эсцину меньше по сравнению с перечисленными венотониками, что указывает на необратную венодилатацию под влиянием эсцина (F. Annoni и соавт., 1979). На перфузированной подкожной вене собак венотонизирующее действие эсцина длится более 5 часов, препарат предопределял повышение венозного давления, а также значительно усиливал сократительный эффект норадреналина. В опытах на собаках in vivo продемонстрированы улучшения эластичности бедренной вены (M. Guillaume и F. Padioleau, 1994). Предполагают, что венотонизирующее действие эсцина обусловлено стимуляцией синтеза и высвобождения простагландина F2a в венозной стенке. Но при перфузии изолированных легких крыс раствором, содержащим эсцин, усиливается выделение этого простагландина (F. Berti и соавт., 1977). Важное значение в улучшении венозного кровообращения и предупреждении рефлюкса имеет выраженное влияние эсцина на процесс плотного закрывания венозных клапанов. Применение эсцина позволяет достичь эффекта, который составляет 90% от максимально возможного в результате действия норадреналина.
Повышение тонуса вен облегчает обратный отток крови из тканей к сердцу, улучшает на 70% протекание лимфы через грудной лимфатический проток. Кроме того, при внутривенном введении эсцина уменьшается содержание адреналина в надпочечниках и повышается АД, а при перфузии изолированных надпочечников наблюдается сосудосуживающее действие. Очевидно, объединение этих эффектов также способствует проявлению противоотечного действия эсцина.
Венотонизирующая и противовоспалительная активность эсцина обеспечивает его терапевтический эффект при варикозной болезни. В возникновении варикозного расширения вен важное значение играет не только венозный стаз, но и активация эндотелиоцитов в условиях гипоксии. На модели ex vivo перфузированной в условиях гипоксии изолированной пупочной вены человека показано, что эсцин тормозит два важных события, которые являются предпосылками активации эндотелиоцитов при гипоксии. Он противодействует уменьшению содержания в эндотелиоцитах АТФ и последующей активации фосфолипазы А2 — фермента, обеспечивающего высвобождение из клеточных мембран предшественника фактора активации тромбоцитов (ФАТ) и арахидоновой кислоты — предшественника модуляторов воспаления — лейкотриенов и простагландинов. С помощью сканирующей электронной микроскопии продемонстрированы угнетения адгезии нейтрофилов и нейтрофилоподобных клеток линии HL60 к венозной стенке в присутствии эсцина. Угнетение гипоксической активации эндотелиоцитов венозной стенки проявлялось при концентрации эсцина 100 нг/мл и достигало максимума при концентрации 750 нг/мл (T. Arnould и соавт., 1996). При этом в системе уменьшалась продукция анионов супероксида и лейкотриена В4 (C. Bougelet и соавт., 1998). Антирадикальные свойства эсцина подтверждены и другими исследователями — он дозозависимо угнетал ферментативное и неферментативное перекисное окисление липидов in vitro (ЕС 5–500 мкг/мл) (M. Guillaume и F. Padioleau, 1994). Таким образом, приведенные результаты экспериментальных исследований свидетельствуют, что эсцин угнетает индуцированную гипоксией активацию эндотелиоцитов, которая предопределяет усиление адгезии нейтрофилов, а их медиаторы и протеазы способствуют разрушению межклеточного матрикса и вызывают повреждения венозной стенки, которые по микроскопическому характеру напоминают изменения, наблюдаемые при варикозной болезни. Уменьшая проявления воспаления и повреждения венозной стенки, эсцин тормозит высвобождение активированными клетками факторов роста, участвующих в пролиферативной фазе воспаления, способствующих сохранению венозной недостаточности и развитию варикоза (R. W. Frick, 2000). Эсцин поддерживает в интактном состоянии эндотелий в условиях венозного стаза, предупреждает рекрутирование, адгезию и активацию нейтрофилов, выступает в роли антагониста медиаторов воспаления, чем предотвращает повреждение венозной стенки. Эти данные, наряду с результатами изучения венотонизирующей активности, еще раз подчеркивают особую ценность профилактического применения препаратов эсцина на ранних этапах варикозной болезни.
Важно, что другие биологически активные вещества, содержащиеся в суммарных вытяжках каштана, потенцируют противовоспалительное действие эсцина. Так, в присутствии естественного флавоноидного комплекса каштана (1:10) активность эсцина усиливается в 5 раз. Противовоспалительными свойствами обладает также петролейный экстракт коры каштана (F. Senatore и соавт., 1989).
Антиэкссудативные и капилляроукрепляющие свойства эсцина обусловливают возможность его применения при отеке мозга, что было впервые доказано экспериментально в 1967 г. S. Gorini и R. Caponi на животных с отеком мозга вследствие краниотомии. Дальнейшие экспериментальные исследования подтвердили эффективность препарата при отеках мозга травматического (T. Tzonos и H. Riebeling, 1968; L. Auer, 1975) и ишемического (M. Cerisoli соавт., 1981) генеза. Для черепно-мозговых травм характерен вазогенный отек мозга, в основе которого лежит повышение сосудистой проницаемости.
В дальнейшем он усугубляется цитотоксическим отеком — набуханием ткани мозга, в основе которого лежат метаболические нарушения, обусловленные собственно травматическим фактором, вазогенным отеком мозга и токсическим влиянием продуктов распада тканей. Медленная резорбция крови из ткани мозга и полости черепа способствует накоплению недоокисленных и токсичных продуктов распада тканей, повышению осмолярности и гидратации (отека и набухания) как локально в месте повреждения, так во всем мозге. Эти процессы приводят к увеличению очага поражения, развитию или увеличению внутричерепной гипертензии, компрессии и смещению мозга. Отек мозга и внутричерепная гипертензия всегда сопровождаются снижением тонуса вен, нарушением венозного оттока, застоем венозной крови в полости черепа с развитием венозной гипертензии, которая способствует развитию деструктивного отека. За счет восстановления поврежденной сосудистой проницаемости и повышения тонуса вен эсцин предотвращает развитие или устраняет нарушения венозного оттока, венозную гипертензию и отек мозга. Уменьшение явлений отека мозга и улучшение венозного оттока, кроме того, способствуют нормализации мозгового кровообращения, что в свою очередь создает благоприятные условия для скорейшего рассасывания (резорбции) очага контузии мозга и гематомы. Ликвидируя нарушения проницаемости сосудистой стенки и повышая тонус вен, а также устраняя отек разных структур мозга, эсцин в значительной мере предотвращает развитие патофизиологических механизмов, лежащих в основе болевых раздражений, и таким образом проявляет анальгезирующий эффект.
Эсцины Ia, Ib, IIa и IIb усиливают эвакуаторную функцию желудка мышей (H. Matsuda и соавт., 2000), угнетают (особенно эсцины IIa и IIb ) всасывание алкоголя в желудочно-кишечном тракте крыс (N. Murakami и I. Kitagawa, 1994).
При пероральном введении мышам (10–50 мг/кг) эсцины Ia, Ib, IIa и IIb заметно угнетают развитие повреждения желудка этанолом (H. Matsuda и соавт., 1999). Гастропротекторный эффект эсцинов угнетается на фоне введения животным капсаицина (который блокирует афферентные вегетативные нервные волокна), метилового эфира N(G)-нитро-L-аргинина (ингибитора NO-синтазы) и индометацина (ингибитора синтеза простагландинов), а также у животных со стрептозоциновым диабетом (с аномальной активностью симпатической нервной системы). Деацилированные производные эсцинов в этом отношении не активны. На на перфузированном желудке наркотизированных крыс продемонстрирована способность эсцина (в дозах 10 и 50 мг/кг) угнетать секрецию соляной кислоты, стимулированную гистамином и карбахолом (E. Marhuenda и соавт., 1994). E. Marhuenda и соавт. (1994) отмечают, что индометацин нивелирует эффект эсцина при этаноловом повреждении слизистой желудка, но они не обнаружили повышения продукции простагландина Е2. Таким образом, механизмы гастропротективного действия эсцина окончательно не выяснены. Очевидно, оно обусловлено частично антисекреторной активностью препарата, а частично опосредуется эндогенными простагландинами, оксидом азота, чувствительными к капсаицину афферентными нейронами и симпатической нервной системой.
Эсцины Ia, Ib, IIa и IIb проявляют гипогликемическое действие в опытах на животных при пероральной нагрузке глюкозой (N. Murakami и I. Kitagawa, 1994; M. Yoshikawa и соавт., 1996). У нормальных животных, а также при введении глюкозы интраперитонеально гипогликемический эффект эсцинов не проявляется. Установлено, что эсцины Ia и IIa не обладают инсулиноподобной активностью и не могут стимулировать выработку инсулина. Их гипогликемический эффект связывают с угнетением всасывания глюкозы в тонком кишечнике (H. Matsuda и соавт., 1998).
Эскулозид (эскулин) благодаря угнетению активности гиалуронидазы стабилизирует капилляры, стимулирует антитромботическую активность сыворотки крови, блокирует угнетение синтеза антитромбина клетками ретикуло-эндотелиальной системы. Эсцин также улучшает реологические свойства крови. Благодаря этому препараты каштана конского способствуют венозному оттоку, улучшают микроциркуляцию, противодействуют возникновению стаза в капиллярах, благоприятно влияют на трофику тканей. Нормализация равновесия между внутрисосудистым давлением и прочностью стенки сосудов предупреждает возникновение кровоизлияний.
Антикоагулянтный эффект препаратов каштана конского связан также с фраксином. Но в целом по антикоагулянтным свойствам они уступают дикумарину.
В опытах in vitro эсцин в концентрации более 10 мкг/мл заметно уменьшает период кристаллизации мочевой кислоты. В опытах на крысах эскулозид проявляет умеренную салуретическую активность, дозозависимо повышая уровень почечной экскреции хлоридов, натрия и калия. Диуретическая активность эсцина значительно слабее, в самой высокой исследуемой дозе достигается минимальный эффект эскулозида (M. J. Martin и соавт., 1990).
В эксперименте продемонстрировано слабое спазмолитическое (папавериноподобное) действие эскулетина, эскулина, фраксина и фраксетина на гладкую мускулатуру внутренних органов и коронарных сосудов.
Сапонины, содержащиеся в препаратах каштана конского, способствуют снижению артериального давления.
Опыты на крысах свидетельствуют, что катехиновый димер проантоцианидин-А2 коры каштана улучшает трофику скелетных мышц в норме и после их травматической денервации (P. Ambrogini и соавт., 1995).
Существуют данные, что сапонины (в частности, эскулетин) и соединения пептидной природы плодов каштана угнетают рост некоторых бактерий и грибов. Эсцины IVc, IVd, IVe и IVf семени Aesculus chinensis обладают свойствами ингибиторов протеазы ВОЛ-1 (X. W. Yang и соавт., 1999).
Экстракт каштана при внутрибрюшинном введении тормозит рост имплантированной мышам асцитной карциномы Эрлиха и лимфосаркомы 150, а при исследовании на курином эмбрионе — лимфосаркомы и карциномы С3Н. Установлено, что он не обладает антимитотической активностью, но уже после кратковременной инкубации с опухолевыми клетками (на протяжении 30 секунд) вызывает в них необратимые морфологические изменения. Установлено, что противоопухолевые свойства экстракта каштана в отношении клеток линии КВ связаны с сапониновой фракцией, в частности с полученными при ее кислотном гидролизе сапогенолами гипокаэскулином и барингтогенол-С-21-ангелатом (T. Konoshima и K. H. Lee, 1986).
При местном применении (накожно) эсцина и меченого 3Н-эсцината натрия в опытах на мышах, крысах и свиньях доказано, что он быстро проникает в близлежащие участки кожи и мышцы. Резорбция эсцина во внутренние органы, кровь, мочу, кожу и мышцы других участков ограничена. Концентрация меченого эсцина в дерме в 50–600 раз, а в мышцах — в 10–50 раз выше, чем в крови. Только 0,5–1% эсцина выводится с мочой на протяжении 24 часов. Подсчитано, что общая элиминация препарата с мочой и желчью составляет 1–2,5% от введенной дозы (W. Lang, 1977). При внутривенном введении эсцин быстро выводится из организма с мочой и желчью, а при пероральном применении сравнительно быстро всасывается преимущественно из двенадцатиперстной кишки.
Разработаны методики радиоиммунного и иммуноферментного анализа концентрации эсцина в сыворотке крови с целью изучения биодоступности и фармакокинетики его препаратов (T. Lehtola и A. Huhtikangas, 1990; C. Hentschel и соавт., 1994).
Токсикология и побочное действие каштана конского
Каштан конский не относится к абсолютно безопасным растениям. Известны случаи смертельного отравления детей его семенем. Токсичность растения обусловлена алкалоидами, гликозидами и сапонинами. При отравлении каштаном наблюдаются: нервное подергивание мышц, слабость, потеря координации движений, расширение зрачков, рвота, диарея, депрессия, паралич и ступор. При отравлении рекомендуется промывание желудка и симптоматическая терапия.
Эсцин, как и другие сапонины, обладает гемолитической активностью, но в терапевтических дозах она не проявляется. Рассчитано, что при применении человеком массой 70 кг таблетки, которая содержит 20 мг эсцина, средняя его концентрация в плазме составляет 0,3 мкг/мл, что в 10 раз меньше концентрации, допустимой для эритроцитов, которая была установлена с помощью метода спиновых зондов (Л. В. Иванов и соавт., 1988).
В эксперименте на крысах показано, что пероральное введение эсцина в дозах 10 и 70 мг/кг не вызывает существенных изменений метаболической функции печени, не усиливает липидный и углеводный обмен (O. Ulicna и соавт., 1993).
Препараты каштана конского обыкновенного хорошо переносятся пациентами, но у отдельных лиц могут вызывать аллергические реакции (зуд, сыпь на коже, крапивница и даже анафилактический шок). Изредка наблюдаются ощущение жара, тахикардия, меноррагии, симптомы раздражения слизистой оболочки желудочно-кишечного тракта, тошнота, изжога, боль в эпигастрии, которые исчезают при уменьшении дозы. Повреждающее действие эсцина на функцию почек в эксперименте не выявлено. Но в клинике после внутривенных инъекций эсцина были описаны нарушения функции почек у детей (даже со смертельным исходом), связанные с передозировкой препарата. У отдельных пациентов с хроническим гепатохолециститом при назначении эсцина возможно кратковременное повышение активности трансаминаз и билирубина (прямой фракции), что не наблюдается при дальнейшем лечении или по его окончании, не составляет угрозы для больных и не нуждается в отмене препарата.
Лекарственные средства каштана, и в частности эсцин, противопоказаны при кровотечениях, тяжелых заболеваниях почек, хронической почечной недостаточности, в первом триместре беременности, гиперчувствительности к его компонентам. Их не следует применять одновременно с аминогликозидами, так как это может повышать нефротоксичность (E. Voigt и H. Junger, 1978). При необходимости одновременного назначения с антикоагулянтами дозу последних следует снижать (под контролем протромбинового индекса). Связывание эсцина с белками плазмы крови затрудняется при одновременном применении антибиотиков цефалоспоринового ряда, что может повысить концентрацию свободного эсцина в крови с риском развития побочных эффектов последнего.
Пыльца цветков каштана может быть аллергеном (W. Popp и соавт., 1992). На основе определения специфического Ig установлено, что частота сенсибилизации пыльцой достигает 12,6% среди детей — городских жителей и 1,9% среди детей сельской местности. Проявления аллергической симптоматики в период цветения каштана совпадают с присутствием специфического Ig в 5,1% городских и 1,4% сельских жителей.
Клиническое применение каштана конского
Многочисленные экспериментальные исследования позволили рекомендовать препараты каштана конского к клинической апробации, а затем — к широкому применению в медицине. Их используют для профилактики и лечения различных сосудистых заболеваний: послеоперационных тромбозов, посттравматических отеков, воспаления и тромбоэмболий.
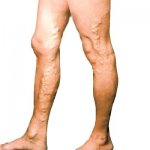
Препараты каштана (эскузан, экстракт или спиртовая настойка плодов) применяются как антигеморроидальное средство, при венозных стазах, варикозном расширении вен, острых и хронических тромбофлебитах, трофических язвах голени. У пациентов с варикозным синдромом после приема препарата уменьшаются отек и воспаление, происходит рассасывание тромбов. Аналогичные эффекты наблюдаются при геморрое. В связи с ускорением кровотока стимулируется процесс очищения трофических язв голени, улучшается тромболизис.
За счет сильного венотонизирующего действия эскузан восстанавливает нормальную циркуляцию крови в венозных сосудах и предупреждает развитие декомпенсации варикозной болезни. Антиагрегантное и антикоагулянтное действие препарата обусловливают его эффективность для профилактики тромбозов. Противовоспалительные, противоотечные и капилляроукрепляющие свойства, способность уменьшать проницаемость плазмолимфатического барьера способствуют быстрой ликвидации клинической симптоматики.
Анализ слепых клинических исследований применения препаратов каштана конского при хронической венозной недостаточности свидетельствует, что после проведенного курса лечения у пациентов уменьшались ощущение усталости и напряженности, зуд, боли в конечностях, отечность голени, лодыжки. Эффективность данных препаратов подтверждена также методами дуплекс-сонографии (M. Ludwig и K. Glanzer, 1987), плетизмографии (L. Pedrini и B. I. Cifiello, 1983), телетермографии (P. Rocco, 1980), реографии (G. Tumino и соавт., 1987) и допплерографическими исследованиями (E. Severin и G. Mladovan, 1988).
Назначение эскузана беременным женщинам с неосложненной варикозной болезнью (по 60 мг 3 раза в день в течение 2 месяцев с переходом на поддерживающую дозу по 40 мг 3 раза в день накануне родов и 1 месяца после) значительно улучшает показатели функции системы гемостаза: увеличивает время рекальцификации плазмы, повышает толерантность плазмы к гепарину, повышает активность антитромбина, способствует ликвидации тромбоцитопении (И. С. Золотухин и соавт., 2000). В 97,5% пациенток наблюдалась положительная клиническая динамика (исчезновение болей и отеков, уменьшение количества варикозных узлов и их напряжение), в то время как в контрольной группе (плацебо) 75% пациенток не отметили клинического улучшения, а у 25% наблюдались симптомы прогрессирования болезни. Осложнения беременности (в основном фетоплацентарная недостаточность, переэклампсия легкой степени) при применении эскузана встречались значительно реже — 15% против 61% в контроле. Эффективным при застойных венозных явлениях у беременных и роженец является также препарат «Веностазин» (содержит экстракт плодов каштана конского и витамин В1), который стимулирует антитромботическую активность сыворотки крови.
Системное стимулирующее влияние эскузана на мозговое кровообращение, гемоциркуляцию в фетоплацентарном комплексе и почках наряду с выявленным антигипертензивным действием позволяют рекомендовать его при беременности, осложненной гестозами, токсико-дисциркуляторной энцефалопатией, фетоплацентарной недостаточностью, хронической внутриутробной гипоксией плода — как в сочетании с варикозной болезнью, так и без нее.
Клинические исследования с применением меченого 125J фибриногена продемонстрировали эффективность эсцина в профилактике послеоперационных тромбозов вен конечностей (H. J. Prexl и соавт., 1976). Профилактическое назначение эсцина, эскузана и эсфлазида в послеоперационном периоде позволило уменьшить на 50% частоту острых тромбозов у пациентов. Препараты каштана конского используют также при нарушениях периферического артериального кровообращения (атеросклерозе сосудов конечностей, артериите, тромбоэмболии мелких сосудов). Описаны случаи выздоровления больных с тромбозом центральных вен сетчатки при лечении веностазином.
Распространенными являются формы препаратов каштана для местного применения — мази, гели, лечебные кремы. Для усиления терапевтического эффекта в Румынии запатентована мазь, содержащая экстракты цветков и семени каштана и цветков арники в соотношении 2:1:1. Двойное слепое клиническое исследование на добровольцах показало эффективность геля 2% эсцина при местном лечении гематом (C. Calabrese и P. Preston, 1993). Препараты эсцина (в частности репарил-гель Н) хорошо зарекомендовали себя при лечении травм конечностей у спортсменов (J. M. Crielaard и соавт., 1986; H. Pabst и M. W. Kleine, 1986; H. Pabst и соавт., 2001), а также в пластической хирургии (E. Janackova, 1977). Методом термографии подтверждена эффективность эсцина при послеоперационных отеках и инфильтратах. При применении репарила температура кожи пациентов в местах поражения нормализовалась в среднем через 2 дня, в контроле — через 4 дня (K. Wilhelm и C. Feldmeier, 1977).
Препараты эсцина используют также для лечения лимфо- и веностатических явлений при опухолях малого таза (P. Schreiner и I. Manka, 1978) и после мастэктомии (D. Dini и соавт., 1981), для профилактики отека гортани при продолжительной интубации трахеи (L. Torelli, 1969), простатита (A. Г. Горбачев и Л. И. Агулянский, 1988) и герпеса, в том числе герпетических поражений глаз (A. Giannetti и C. Pelfini, 1968).
Важной сферой применения эсцина является нейрохирургия и неврология. Клинические наблюдения, проведенные еще в 60–70-х годах немецкими и итальянскими учеными, продемонстрировали терапевтическую эффективность эсцина при цереброваскулярной недостаточности (G. Feine-Haake и соавт., 1975), травматических повреждениях спинного мозга (G. C. Serra и соавт., 1969), черепно-мозговых травмах (H. E. Diemath и H. Spatz, 1976; R. Hemmer, 1985), травматическом отеке мозга (H. E. Diemath, 1975, 1981; F. Heppner и соавт., 1976), послеоперационных отеках мозга в связи с нарушением циркуляции ликвора (M. Scanarini и соавт., 1979), для ликвидации явлений отека мозга у пациентов с опухолями в предоперационном периоде (S. Mingrino и M. Scanarini, 1978). Положительные результаты такого лечения подтверждены результатами клинического наблюдения за пациентами, а также данными энцефалографии (C. Rivano и G. Rosadini, 1969). Применение эсцината натрия при травматическом отеке мозга способствовало нормализации повышенного внутричерепного давления (от 250–500 мм вод. ст. до 150 мм вод. ст.) и сокращению времени потери сознания. Дальнейшие наблюдения за пациентами в течение 2 лет (максимально 3,5 лет) после травмы и лечения продемонстрировали уменьшение периода реабилитации (T. R. Put, 1979). В 73,3% пациентов с доброкачественным повышением внутричерепного давления (псевдоопухолей мозга) ведение эсцината натрия (по 20 мг внутрь через каждые 8 часов в течение 3 дней с последующим применением аналогичной дозы препарата per os) приводило к нормализации краниального давления и изменений на глазном дне, ремиссии клинического синдрома. На протяжении года у них не наблюдалось рецидивов заболевания (S. Mingrino и соавт., 1980).
В Украине создан инъекционный препарат — L-лизина эсцинат (аналог немецкого препарата «Репарил») для лечения посттравматических и послеоперационных отеков. Его применяют также при контузиях, сотрясениях мозга, в тяжелых случаях нарушения венозного кровообращения. Разработанная на АО «Галычфарм» (Львов) технология изготовления 0,1% раствора L-лизина эсцината для инъекций обеспечивает стабильность препарата на протяжении 2 лет.
В клинике Института нейрохирургии АМН Украины им. акад. А. П. Ромоданова проведено изучение клинической эффективности L-лизина эсцината на 30 больных с тяжелой черепно-мозговой травмой, ушибом головного мозга тяжелой степени и сопутствующим отеком мозга, внутричерепными кровоизлияниями различного характера и степени выраженности, переломами костей свода и основания черепа (П. Спасиченко, 2001). Установлено, что препарат проявляет выраженное и быстрое противоопухолевое действие. У пациентов с травматическим отеком мозга он ликвидирует или значительно уменьшает явления отека и набухания головного мозга и мозговых оболочек, устраняет сжатие и смещение структур мозга, ускоряет рассасывание очагов контузии мозга, включая их геморрагический компонент, ликвидирует внутричерепную гипертензию. Препарат не только устраняет перечисленные явления, но и предотвращает их развитие.
Уменьшая отек головного мозга и предупреждая его развитие, препарат способствует быстрому регрессу клинической симптоматики и восстановлению функциональной активности головного мозга. Это проявляется значительным улучшением общего состояния пациентов, уменьшением степени нарушения сознания и очаговых неврологических нарушений (пробковых и проводниковых), улучшением или нормализацией двигательных, психоэмоциональных и интеллектуально-мнестических функций, памяти, ориентирование на месте, во времени и обстоятельствах. У пациентов на фоне лечения L-лизина эсцинатом быстро регрессирует или вообще не развивается менингеальный синдром, нормализуется спинномозговое давление и исчезают явления застоя на глазном дне. При эхоэнцефалоскопии отмечается нормализация положения и ширины срединного эхо-сигнала. Данные компьютерной томографии головного мозга подтверждают развитие выраженного и быстрого противоопухолевого эффекта — уменьшается перифокальная зона отека и его выраженность, ликвидируется сжатие и смещение цистерн, желудочковой системы мозга и серединных структур.
За счет выраженного противоотечного и венотонизирующего действия L-лизина эсцинат дает возможность избежать травматического оперативного вмешательства, провести консервативное лечение и предотвратить возможное развитие различных осложнений. В связи с этим при черепно-мозговых травмах препарат необходимо вводить как можно раньше — сразу после госпитализации больного в стационар или на догоспитальном этапе. Кроме того, L-лизина эсцинат предотвращает развитие отека мозга при нарушении мозгового кровообращения вследствие блокады пробкового сосуда во время оперативного вмешательства. Таким образом, L-лизина эсцинат открывает новые возможности в лечении больных с тяжелой черепно-мозговой травмой. Предполагается его эффективность при лечении отека мозга у пациентов с ишемическими нарушениями и опухолевыми поражениями мозга. Установлен выраженный анальгетический эффект L-лизина эсцината при наличии болевого синдрома травматического генеза, особенно головной боли.
За счет гипогликемического действия L-лизина эсцинат у пациентов с повреждением мозга ликвидирует стрессовую гипергликемию и нормализует уровень углеводов в крови, что предотвращает развитие или устраняет явления ацидоза мозга и усугубление церебрального дефекта.
Характерной особенностью препарата является выраженная иммуномодулирующая активность. Он повышает и нормализует как относительное, так и абсолютное количество лимфоцитов, повышает уровень γ-глобулинов в крови, нормализует содержание α- и β-глобулинов. Таким образом L-лизина эсцинат повышает защитные силы организма. Ни у одного больного, леченного L-лизина эсцинатом, в посттравматическом периоде не развились осложнения воспалительного характера. Это препарат очень выгодно отличается от кортикостероидов.
Клинические исследования, выполненные в Украинском НИИ травматологии и ортопедии и Харьковском НИИ ортопедии и травматологи им. проф. М. И. Ситенка, доказали высокую эффективность препарата при отечно-болевом синдроме у пациентов после операций по поводу травм и заболеваний опорно-двигательного аппарата, а также у больных с нейродистрофическим синдромом. Для предупреждения или уменьшения отека спинного мозга раствор L-лизина эсцината рекомендуется пациентам с осложненной травмой позвоночника в раннем послеоперационном периоде. Препарат проявляет также анальгетическое действие при болевом синдроме травматического генеза, включая головные боли, способствует быстрой резорбции травматического отека мягких тканей черепа, лица, конечностей, туловища.
Препарат «Эсфлазид» (смесь эсцина и флавазида) проявляет эффект, аналогичный эсцину, но обладает меньшим гемолитическим индексом и токсичностью.
Благодаря седативным свойствам препараты каштана могут быть эффективными при ряде заболеваний нервной системы (ипохондрии, истерии).
Экстракт плодов каштана конского входит в состав запатентованной в Японии фитокомпозиции для предупреждения мутаций в клетках желудка и кишечника, индуцированных 1-метил-1-нитрозомочевинной, N-метил-N’-нитро-N-нитрозогуанидином и другими канцерогенами (K. Sudzuki и соавт., 1987).
В гомеопатию препараты каштана были введены Гелбигом (Gelbig) после проведенных испытаний на здоровых добровольцах. Их назначают при нарушениях венозного кровообращения: ощущении полноты и пульсации в венах, тяжести и болей в области печени, поясничной и крестцовой областях, ощущениях сухости, жара и колющих болей в горле и прямой кишке, тяжести и болях в желудке через 3 часа после еды с горькой отрыжкой и изжогой, а также при расширении вен глазного дна с ощущениями болей, тяжести и жара в глазах.
Лекарственные средства каштана конского
Сбор противогеморроидальный (Species antihaemorroidale) — содержит 3 части плодов каштана конского, 3 части цветков ромашки аптечной, 3 части травы шалфея и 5 частей коры дуба. Обладает противовоспалительными и антисептическими свойствами. Применяют для сидячих ванн (4 столовые ложки сбора заваривают 3 стаканами кипятка, настаивают в термосе 2 часа, процеживают и разводят водой до 2 л).
Эскувазин (Aescuvasin, Болгария) — спиртовой экстракт плодов каштана конского в виде капель. Употребляют по 20 капель 3 раза в день при варикозном расширении вен, тромбофлебитах, трофических язвах голени, геморрое.
Aescuvasin compositum (Болгария) — спиртово-водные экстракты из плодов каштана конского и рябины обыкновенной. Употребляют по 10–15 капель 3 раза в день при капиллярных кровоизлияниях, варикозном расширении вен, тромбофлебитах, флебитах, геморрое.
Эсцин (Aescin, Polfa-Kutno, Польша) — таблетки, покрытые оболочкой, которые содержат 20 мг аморфного эсцина. Применяется как противовоспалительное, противоотечное и антитромботическое средство при посттравматических и послеоперационных отеках, травматических повреждениях, обширных посттравматических гематомах, заболеваниях вен нижних конечностей у пациентов с недостаточностью кровообращения, заболеваниях шейного отдела позвоночника с корешковым синдромом, а также для предупреждения послеоперационных гематом. Применяют по 3 таблетки 3 раза в сутки после еды с достаточным количеством жидкости.
Побочное действие: возможны ощущения жара, тошнота, тахикардия, зуд, высыпания на коже, крапивница. Препарат противопоказан при тяжелых заболеваниях почек, хронической почечной недостаточности, в первом триместре беременности, гиперчувствительности к его компонентам.
Применение в промышленности
В прошлом семена конского каштана обыкновенного, содержащие мыльную жидкость (благодаря присутствию сапонинов), использовали во Франции и Швейцарии для отбеливания конопли, льна, шёлка и шерсти. Лён, отмытый в этой жидкости, а затем промытый в проточной воде, приобретал небесно-голубой цвет.
Древесина конского каштана коммерческого значения не имеет, хотя и обладает достаточно высокой прочностью, легко, с минимальной потерей качества сушится. Подходит для изготовления мелких предметов домашнего обихода и поделок, ящичной тары.
Даёт медоносным пчёлам очень много нектара (с содержанием сахара от 65 до 75 %) и пыльцы, а весной — клей (прополис). Мёд, собранный с конского каштана, быстро кристаллизуется в сотах, поэтому его нельзя использовать для зимней подкормки пчёл.
Плоды каштана конского используют для производства женских украшений (бус).
Ивано-Франковская государственная медицинская академия
Фотографии и иллюстрации




Комментариев: 0










 Чтобы сообщить нам о грамматической ошибке на сайте
выделите её и нажмите Ctrl+Enter
Чтобы сообщить нам о грамматической ошибке на сайте
выделите её и нажмите Ctrl+Enter